
België moet zijn sterk ecosysteem voor klinisch onderzoek in de oncologie behouden
België blijft een Europese koploper op het gebied van klinisch onderzoek in de oncologie, maar deze positie wordt steeds kwetsbaarder. Om patiënten toegang te blijven bieden tot innovaties en een erkend ecosysteem van excellentie te behouden, is het essentieel om de aantrekkelijkheid van ons land te behouden en te versterken. Het nieuwe nationale kankerplan biedt een uitgelezen kans om hiervoor een ambitieuze en omvattende strategie te uit te werken en te implementeren.
België behoudt zijn leidende positie in de EU op het gebied van klinische studies, maar die positie is kwetsbaar
Uit een recent rapport van Deloitte voor pharma.be blijkt dat België in 2024 zijn positie als één van de Europese koplopers zal behouden wat betreft het aantal toegestane klinische proeven per inwoner. Het rapport wijst echter op een lichte daling van het aantal vergunningen in België (-1,1 %) in de afgelopen acht jaar en dat, hoewel België nog steeds aan kop gaat, andere lidstaten, zoals Nederland, hun achterstand aan het inhalen zijn. Bovendien verliest Europa in het algemeen terrein op het gebied van klinisch onderzoek.
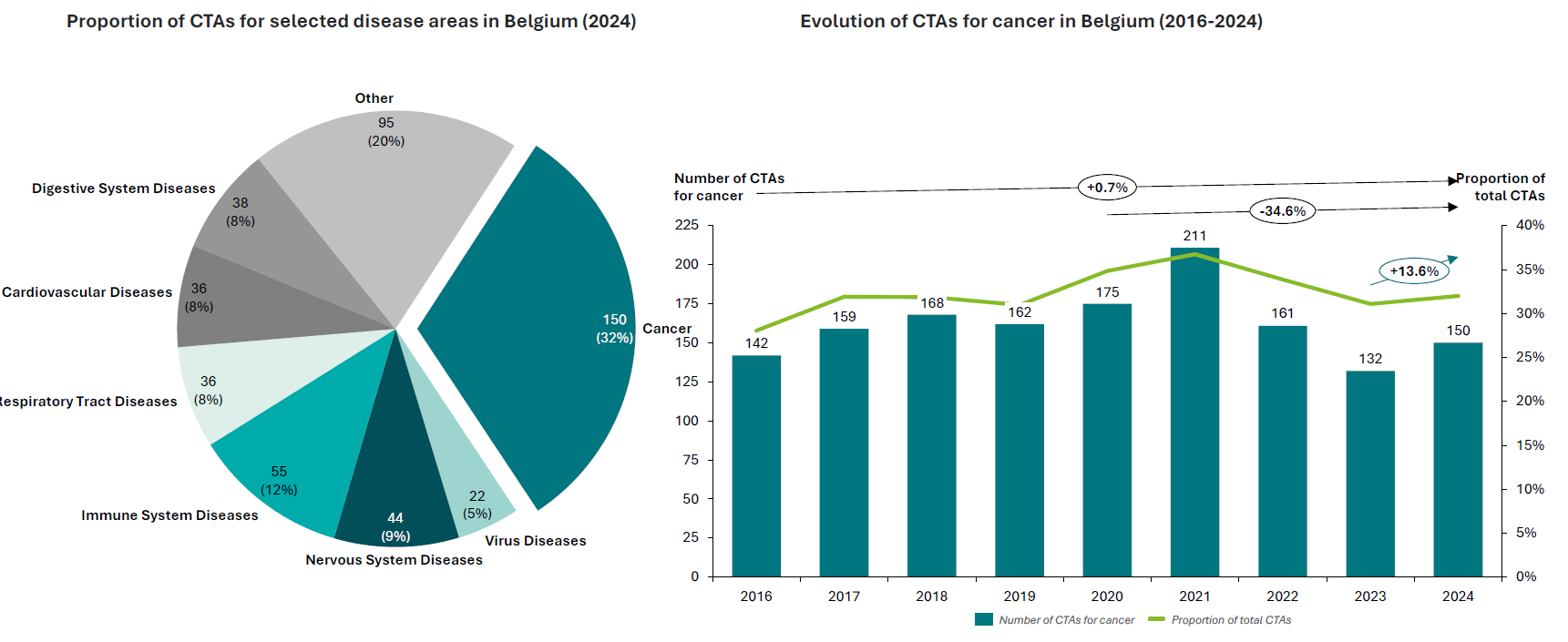
In 2024 zijn 32 % van de in België goedgekeurde studies, oncologische studies, wat de expertise van België op dit gebied illustreert; 17 % van de oncologische studie die in Europa worden uitgevoerd, vindt in België plaats, wat de sterke aanwezigheid van ons land in Europa bevestigt.
Dit solide ecosysteem voor klinische studies in de oncologie in het bijzonder (met hoogwaardige kankerzorg, geavanceerde infrastructuur en belangrijke opinieleiders onder de onderzoekers) moet worden behouden en onze leidende positie moet worden gehandhaafd en, indien mogelijk, verbeterd. De aantrekkelijkheid van ons land voor klinisch onderzoek is cruciaal om Belgische patiënten toegang te geven tot de nieuwste innovaties die hun leven kunnen redden en om onze klinische expertise op Belgisch grondgebied te versterken.
Een flexibel regelgevingskader is essentieel voor gecombineerde klinische studies
Klinische studies die het testen van een nieuw geneesmiddel combineren met een in-vitrodiagnostiek komen steeds vaker voor op het gebied van oncologie. Deze “gecombineerde studies” zijn complex om te beoordelen, omdat ze verschillende wetgevingen met zich meebrengen die niet op elkaar zijn afgestemd. Dit leidt tot vertragingen bij de start van deze studies en bij de toekomstige toegang tot innovatieve geneesmiddelen op het gebied van oncologie. Het Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten (FAGG) heeft in januari 2026 de invoering aangekondigd van een vereenvoudigde en geharmoniseerde procedure voor de beoordeling van deze gecombineerde studies, om de beoordeling ervan en bijgevolg ook de start ervan in België te vergemakkelijken.
Investeren in Real World Data (RWD) om klinische studies in België te behouden
Een optimaal gebruik van hoogwaardige gegevens is een sleutelfactor voor het verbeteren van de efficiëntie in alle stadia van de klinische ontwikkeling. Toegang tot reële gegevens, bijvoorbeeld via het Agentschap voor gezondheidsgegevens, om de haalbaarheid van studies te optimaliseren en patiënten te identificeren en te rekruteren, en zo snelle en voorspelbare starttermijnen te garanderen, zal België in staat stellen zich te positioneren als een gunstig doelland.
Bovendien zouden de gegevens het gebruik van nieuwe technologieën in klinische studies kunnen vergemakkelijken, waardoor België zich als pionier op het gebied van innovatie zou kunnen positioneren. Daarom voeren we, zoals bepaald in het akkoord van de Belgische federale regering, een systeem voor gegevensuitwisseling in dat voldoet aan de Algemene Verordening Gegevensbescherming (AVG) en compatibel is met de Europese ruimte voor gezondheidsgegevens (EHDS), zodat een vlotte en veilige gegevensuitwisseling de basis vormt voor gecoördineerde en geïntegreerde zorg, met inbegrip van klinisch onderzoek. De Europese ambitie op het gebied van gegevensuitwisseling en AI-technologie (AI-wet) is om Europa aan de top te plaatsen van innovatie in de technologiesectoren die belangrijk zullen zijn voor de economie van morgen (Competitiveness Compass van de Europese Commissie). Bijgevolg investeren verschillende Europese landen actief in data-infrastructuur en -technologieën om meer kwalitatieve real-world data te hergebruiken in onderzoek en gezondheidszorg. Bovendien maakt de toonaangevende Europese regelgevende instantie, het Europees Geneesmiddelenbureau (EMA), gebruik van Real World Data bij het nastreven van haar statutaire doelstellingen, zoals het vergemakkelijken van de ontwikkeling van en de toegang tot geneesmiddelen.
De ontwikkeling van een nationaal netwerk voor klinische studies, met een gegevensnetwerk dat klinische centra met elkaar verbindt, zou een centrale coördinatie van de haalbaarheid van studies en de lokalisatie van patiënten mogelijk maken en zo een efficiënte rekrutering van patiënten garanderen (een zwak punt van het Belgische landschap op het vlak van klinische studies). Een dergelijk netwerk zou ook steunen op de uitwisseling van expertise tussen klinische centra en onderzoekers, een expertise die bijzonder wordt erkend als een troef voor ons land en die meer zou moeten worden benut. Dit moet dan ook een van de prioritaire acties zijn van het nieuwe nationale kankerplan en de diens ambitieuze omvattende strategie rond data en klinische onderzoek opdat België zijn leidende positie in klinische onderzoek in oncologie zou kunnen behouden.



Schrijf je in op onze nieuwsbrief
Wil je op de hoogte blijven van het reilen en zeilen binnen de farma-industrie, schrijf je dan in op onze nieuwsbrief!


