
29 février 2024 - Journée des maladies rares
La Journée des maladies rares (« Rare Disease Day ») a également lieu dans le monde entier le 29 février de cette année. L'objectif est de sensibiliser le public aux maladies rares et aux nombreuses personnes qui en sont atteintes, et de stimuler ainsi la recherche de traitements efficaces.
La première Journée des maladies rares a été organisée par l'Organisation européenne pour les maladies rares (EURORDIS) et s'est tenue le 29 février 2008. Cette date a été choisie parce que le 29 février est un « jour rare ». En dehors des années bissextiles, la Journée des maladies rares tombe le 28 février.
En Belgique, RaDiOrg - Rare Diseases Belgium représente plus de 80 associations pour des maladies rares spécifiques et compte également des centaines de membres individuels atteints d'une maladie pour laquelle il n'existe pas d'association . Il existe plus de 6 000 maladies rares uniques qui, ensemble, touchent entre 3,5 % et 5,9 % de la population. Entre 500 000 et 700 000 Belges sont atteints d'une maladie rare.
Continuer à innover pour les patients atteints de maladies rares, aujourd'hui et demain
Comment de petits pas peuvent avoir un impact important
Il existe tant de médicaments efficaces, tant d'investissements dans la recherche et le développement de nouveaux médicaments, et en même temps tant de maladies rares que nous ne sommes toujours pas en mesure de traiter de manière adéquate, voire pas du tout. Pourquoi en est-il ainsi et que pouvons-nous faire pour y remédier ?
De grands pas ...
Depuis des décennies, d'innombrables scientifiques dans les universités, les instituts de recherche et les entreprises pharmaceutiques du monde entier s'efforcent de trouver et d'améliorer des solutions efficaces pour lutter contre les maladies, en se basant sur les besoins non satisfaits des patients.
En consultation avec des médecins, des patients et d'autres parties prenantes, les éditeurs biopharmaceutiques innovants b se concentrent uniquement sur le développement de médicaments qui apportent une valeur ajoutée aux patients, aux systèmes de soins de santé ou à la société. Cette approche a permis de guérir un très grand nombre de patients dans le monde entier et/ou d'améliorer considérablement leur qualité de vie au cours des 60 dernières années. Mais le développement de nouveaux médicaments passe par des essais et des erreurs. Pour 10 000 molécules potentiellement prometteuses au tout début du processus de recherche et de développement, seul un médicament parvient à franchir la ligne d'arrivée et à être approuvé par le gouvernement [1].
En effet, les innovations scientifiques ne se produisent pas toujours en ligne droite. Les vaccins COVID-19 à ARNm en sont un exemple récent et réussi. Après tout, la science sous-jacente était déjà en cours de développement au début des années 1990, mais elle était davantage axée sur la lutte contre les tumeurs [2]. Ces longs travaux préliminaires ont permis d'estimer très rapidement le potentiel de vaccination, de sorte que les vaccins COVID-19 ont permis d'éviter au moins 14,4 millions, voire 19,8 millions de décès, dans le monde entier et en une seule année.
... souvent de nombreux petits pas successifs
Pour de nombreuses innovations, cependant, nous observons une succession de petites améliorations pertinentes. Un bon exemple est la baisse régulière mais importante de la mortalité due aux maladies cardiovasculaires entre 1950 et 2010, en partie grâce aux progrès scientifiques constants et à l'arrivée de nouveaux médicaments.
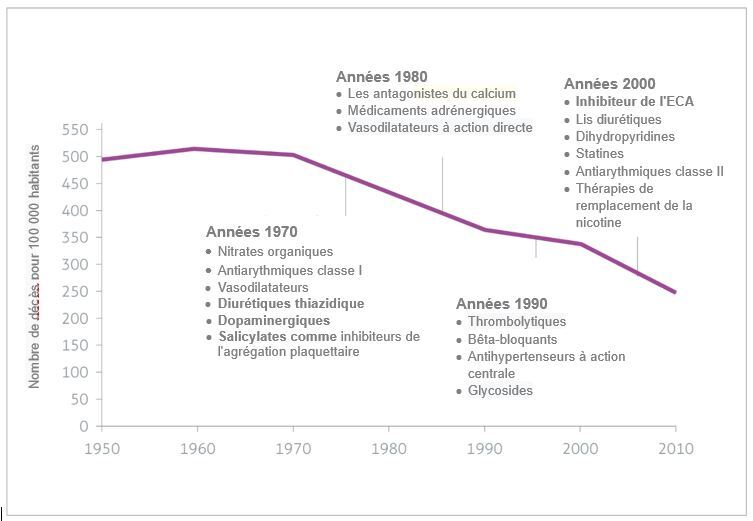
Il en va de même pour d'autres maladies, comme le montre un rapport assez récent sur la Belgique.
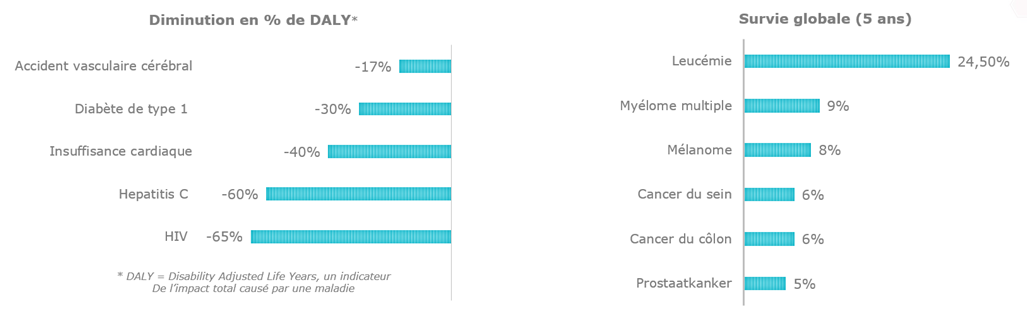
Une autre étude internationale indique que les médicaments innovants seraient responsables de 73 % de l'augmentation de l'espérance de vie dans les pays membres de l'OCDE, dont la Belgique [3].
Il reste encore beaucoup à faire
Malheureusement, la science ne se laisse pas forcer la main. La maladie d'Alzheimer en est un bon exemple. Entre 1995 et 2021, les investissements privés dans la recherche et le développement d'un traitement pour cette maladie se sont élevés à 42,5 milliards de dollars. Mais il n'existe toujours pas de traitement concluant, ni même de guérison.
De nouveaux traitements sont également disponibles pour les maladies rares. En 2022, 24 nouvelles autorisations de mise sur le marché de médicaments orphelins ont été accordées par l'Agence européenne des médicaments (EMA), ce qui porte à 231 le nombre de médicaments pour maladies rares ayant reçu une autorisation de mise sur le marché dans l'Union européenne depuis l'introduction de la législation sur les médicaments orphelins. Dans le même temps, il convient de noter que 6 000 à 8 000 maladies rares sont encore en attente d'un (meilleur) traitement ou d'une guérison. D'autre part, il existe de nombreuses affections pour lesquelles il existe des traitements, mais qui n'aboutissent pas à une guérison ou au rétablissement complet de la qualité de vie.
Pourquoi est-ce si difficile ?
Identifier les besoins médicaux des patients est une chose. Trouver le remède en est une autre, et cela dépend fortement de l'état de la science, tant en termes d'informations sur la cause d'une affection que de mécanisme d'action possible pour un nouveau médicament.
En raison de la nature rare, voire ultra rare, des maladies orphelines, c'est souvent précisément là que l'on manque de connaissances scientifiques suffisantes et de compréhension des causes exactes de la maladie. Le trouble est-il causé par des lésions de l'ADN, est-il héréditaire, quelles chaînes de processus biochimiques dans la cellule sont impliquées ? Sans ces connaissances, il n'est pas non plus possible d'identifier le gène, la protéine ou le processus qui est à l'origine du trouble. Par conséquent, il n'est pas possible d'utiliser une cible spécifique pour commencer à développer un médicament de manière ciblée.
Lorsque ces connaissances sont enfin disponibles, leur conversion en un médicament sûr et efficace est toujours associée à un risque élevé d'échec, à de longs délais de développement (10 à 15 ans) et à des investissements considérables (environ 1,5 milliard d'euros en moyenne).
Parallèlement, les temps de développement, les taux d'échec, les dépenses de recherche et développement (R&D) et les exigences réglementaires au sein du secteur pharmaceutique européen ont augmenté au cours de la même période.
Le déclin de la productivité de la R&D est lié à la concentration des investissements dans des domaines thérapeutiques présentant un risque d'échec plus élevé, et en particulier dans des maladies caractérisées par d'importants besoins non satisfaits et des mécanismes biologiques complexes insuffisamment étudiés [4].
Cependant, la recherche de nouveaux traitements pour les nombreuses maladies encore plus rares est très difficile et entravée par d'importantes taches blanches et d'immenses défis scientifiques. Au rythme actuel, il faudrait plus de 100 ans pour mettre au point des traitements pour toutes les maladies rares. C'est pourquoi la collaboration « Rare Disease Moonshot » a été mise en place pour stimuler la recherche, les essais cliniques et les processus réglementaires grâce à de nouvelles recommandations.
Et même après l'approbation d'un nouveau médicament par le gouvernement, celui-ci n'est pas toujours réellement disponible. Sur l'ensemble des médicaments orphelins innovants approuvés par l'Agence européenne des médicaments (EMA) entre 2018 et 2021, seuls 36 % étaient remboursés aux patients en Belgique au début du mois de janvier 2023 (contre, par exemple, 90 % en Allemagne, 79 % en France ou 46 % aux Pays-Bas) [5].
Que nous réserve l'avenir ?
Étant donné que 95 % des maladies rares ne disposent pas encore de traitements adéquats, il est essentiel que les universitaires, les patients et les décideurs politiques travaillent d'arrache-pied pour l'avenir. Le secteur biopharmaceutique innovant investit chaque jour plus de 15 millions d'euros dans la recherche et le développement. Cela montre que la Belgique ne lésine ni sur les coûts ni sur les risques. La protection temporaire de la recherche et du développement, par exemple au moyen de brevets, permet de continuer à investir dans la recherche de nouveaux médicaments. Par essais et erreurs, pas à pas, parfois grands, parfois petits. Grâce aux progrès rapides de la science et à une médecine de plus en plus personnalisée, plusieurs nouvelles solutions seront disponibles pour les maladies rares dans les décennies à venir. Il est donc important qu'elles trouvent rapidement leur place dans le système de soins de santé soutenu par la nouvelle feuille de route pour l'accès aux nouveaux médicaments, au bénéfice des patients et des citoyens, en particulier mais aussi ceux qui sont atteints de maladies rares.

[1] www.efpia.eu/publications/data-center/the-pharma-industry-in-figures-rd/rd-process/
[2] Press release The Nobel Prize in Physiology or Medicine 2023, www.nobelprize.org/prizes/medicine/2023/press-release/
[3] www.nber.org/system/files/working_papers/w18235/w18235.pdf
[4] Pammolli, F., Magazzini, L., & Riccaboni, M. (2011). The productivity crisis in pharmaceutical R&D. Nature reviews Drug discovery, 10(6), 428-438.
[5] EFPIA Patients W.A.I.T. Indicator 2022 Survey, Published April 2023, www.efpia.eu/media/s4qf1eqo/efpia_ patient_wait_indicator_final_report.pdf

Intéressé(e) à recevoir les nouvelles de pharma.be
Etre au courant de ce qui vit au sein de l'industrie pharmaceutique ? Inscrivez-vous à notre lettre d'information.


