
La Belgique, un pôle pour la recherche clinique
Chaque année depuis 2017, Deloitte effectue pour pharma.be une analyse de l’empreinte des essais cliniques en Belgique et du positionnement du pays au niveau européen. Cette étude fournit non seulement une analyse des statistiques sur les essais cliniques en Belgique, mais donne également une comparaison des caractéristiques entre la Belgique et une sélection de neuf pays européens (Allemagne, Danemark, Espagne, Estonie, France, Pays-Bas, Pologne, Royaume-Uni et Suède).
Un environnement dynamique pour la recherche clinique est essentiel pour faire progresser les soins de santé, et la science au bénéfice des patients, des professionnels de la santé, des chercheurs d’un pays. Cette étude permet d’une part de suivre l’évolution du nombre d’essais cliniques et leurs caractéristiques (phase de recherche, aire thérapeutique) en Belgique au fil des ans, et par conséquent de la compétitivité du pays en Europe en la matière, et d’autre part, de voir comment renforcer l’environnement pour que la Belgique reste un pôle d’essais cliniques.
Découvrez le rapport de Deloitte
La Belgique toujours dans le top 3 européen
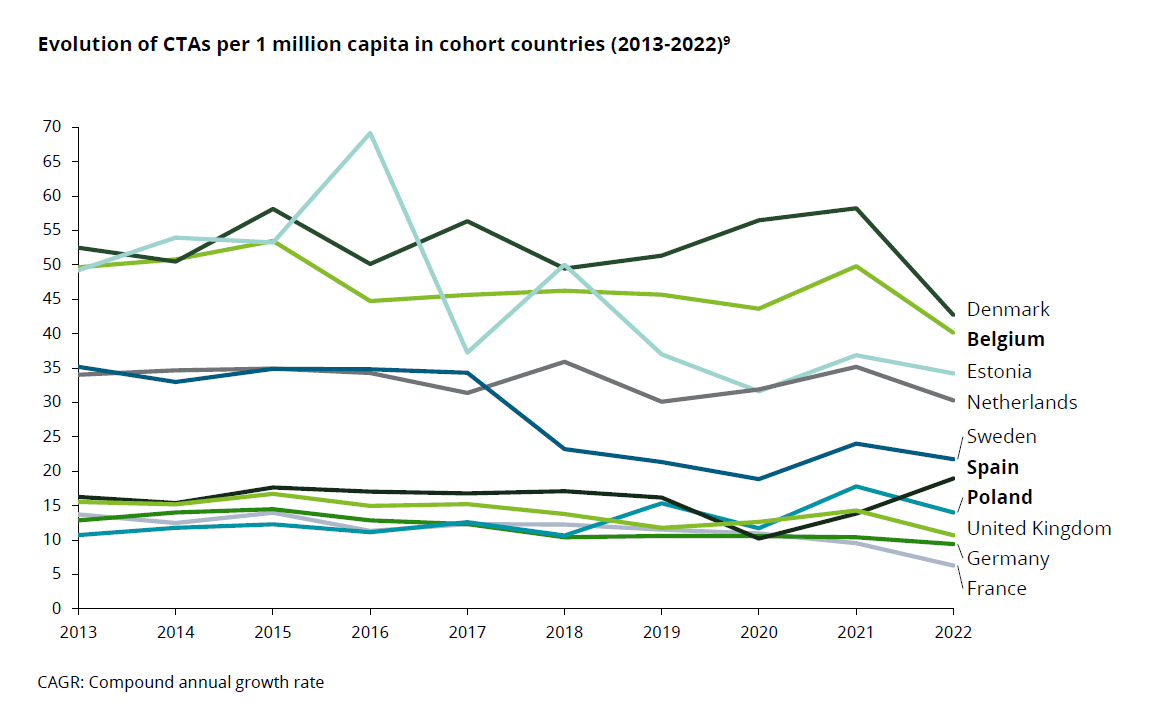
Les patients belges ont jusqu’à présent bénéficié d'un certain avantage en matière d’essais cliniques. Depuis plus de dix ans et jusqu’en 2022, notre pays se maintient dans le top 3 européen quant au nombre de demandes d'essais cliniques par million d’habitants comme illustré ci-dessous.
Cette position privilégiée est en partie due aux entreprises biopharmaceutiques, qui représentent pas moins de 80 % des demandes d'essais cliniques en Belgique. Pour ce faire, elles ont pu compter sur un écosystème solide : la grande qualité de notre monde académique et de nos chercheurs, nos hôpitaux et centres de recherche bien développés ainsi que les connaissances solides et de l’expertise des autorités compétentes sont les forces principales du pays pour y conduire un essai clinique.
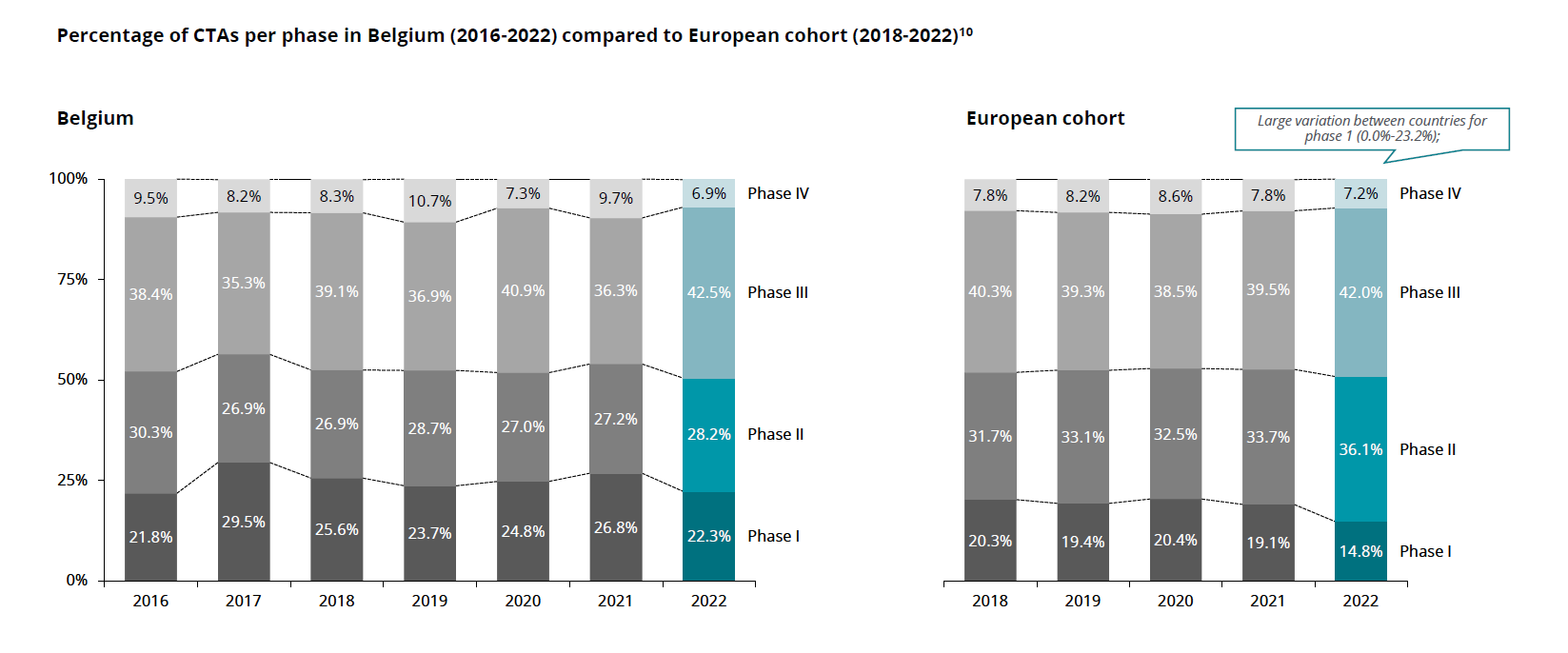
Expertise en matière de phase 1 et First-in Human (FIH)
On observe une solide expertise belge dans les premières phase de développement d’un médicament. La proportion d’essais clinique de phase 1 autorisés en Belgique est supérieure à la moyenne des neufs pays européens examinés. Cette proportion importante, bien que se tassant légèrement ces dernières années, est largement due à une nombre croissant de premiers essais chez l’Homme (ou First-in-Man FIH).

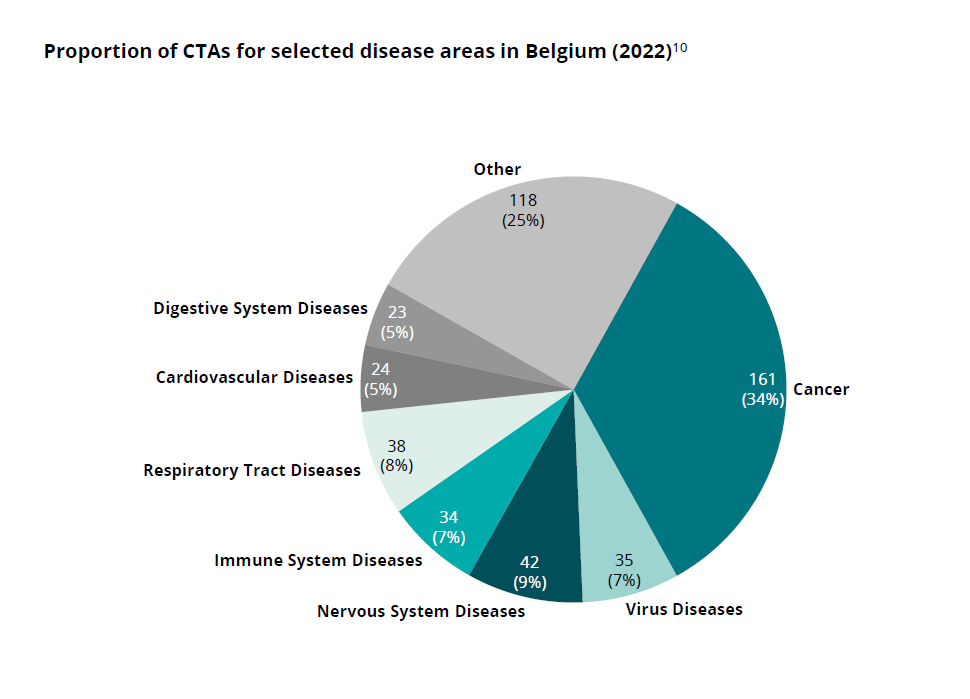
La lutte contre le cancer en tête
Les essais cliniques menés en Belgique concernent une grande variété de domaines thérapeutiques, avec une forte empreinte des essais en cancérologie. Plus d’un essai sur trois autorisé en Belgique en 2022 concerne un traitement contre le cancer, soit un total de 161 nouveaux essais cliniques.
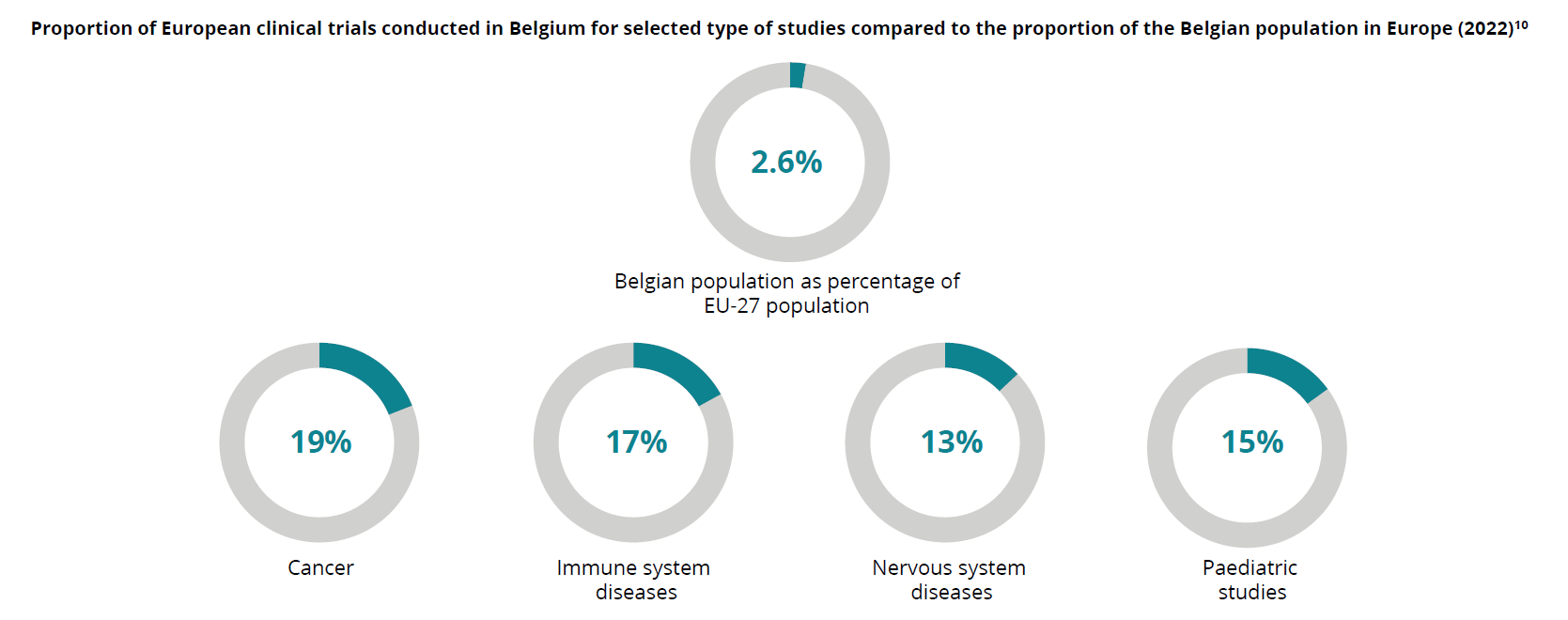
Cette forte empreinte se retrouve au niveau européen puisque 19 % des essais cliniques menés dans la recherche contre le cancer en Europe ont été effectués en Belgique alors que notre pays ne compte que 2,6 % de la population européenne.
Il faut noter également une proportion important d’essais cliniques concernant des traitements de maladies orphelines en Belgique, avec un essai sur quatre autorisé en 2022 dans le domaine des maladies orphelines.
Une position à risque
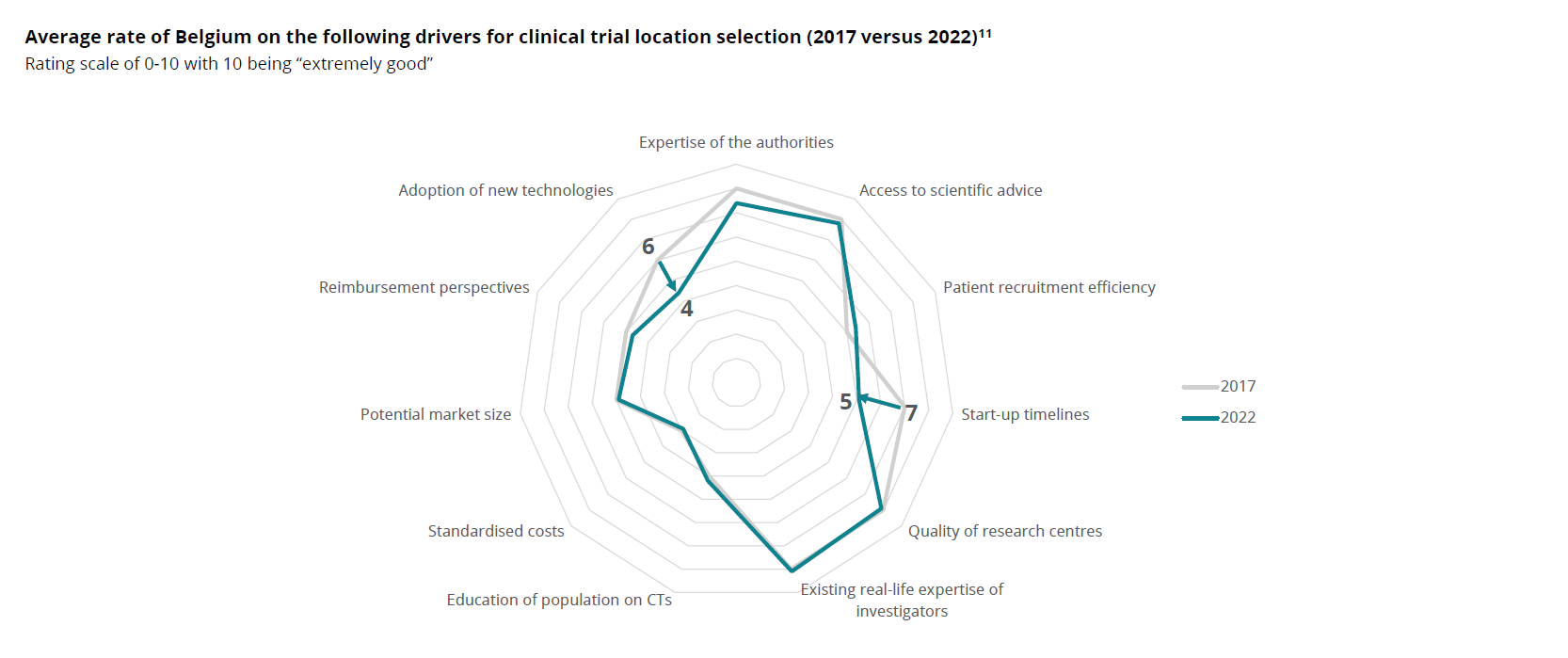
Une forte expertise scientifique et réglementaire ainsi que la qualité des centres d'essais restent des facteurs clés de l'attractivité de la Belgique en 2022. Notre position privilégiée n’est toutefois pas une garantie pour l’avenir. De nombreux pays nous l’envie et la concurrence devient donc féroce. De plus le pays doit s’adapter à l’implémentation d’un nouveau règlement européen en matière d’essais cliniques. On voit que certains des facteurs qui soutenaient le choix de la Belgique pour y conduire les essais deviennent des points d’attention, tels les délais de démarrage d’un essai (notamment suite à l’implémentation du règlement européen), l’adoption d’innovations et nouvelles technologies dans les essais.
La Belgique doit pouvoir se différencier par rapport aux autres pays et régions et construire à partir de ses atouts pour renforcer sa compétitivité en tant que pôle de recherche clinique.
Nous appelons donc au suivi des délais d'évaluation effectifs des demandes d'essais par l'AFMPS, ainsi qu'à une communication active sur les délais courts spécifiques adoptés en Belgique pour les essais mononationaux de phase 1 par l'AFMPS. Ensemble, les parties prenantes doivent également travailler à l’optimisation du processus de démarrage afin d’en assurer la fluidité et la prévisibilité.
En outre, l'AFMPS devrait continuer à investir dans le développement de son expertise ainsi que de ses lignes directrices, et dans le renforcement de son bureau d'innovation pour permettre et faciliter l'utilisation de technologies et méthodologies innovantes dans les essais cliniques. Il devrait y avoir un forum permettant à toutes les parties prenantes en Belgique d'échanger sur les meilleures pratiques et de se tenir au courant des derniers développements scientifiques et technologiques, et d'aider les régulateurs à être au courant des dernières tendances.
Focus sur les questions de diversité
Cette année, l’étude s’est également penchée sur les questions de diversité, d'équité et d'inclusion dans les essais cliniques.
L'objectif est de promouvoir et assurer un accès et une représentation justes et équitables au seins des essais cliniques, afin d'améliorer la généralisation et l'applicabilité des résultats à la population la plus susceptible d’utiliser le traitement ou le médicament dans la pratique. Par représentation juste et équitable, on entend que les participants à la recherche représentent un large éventail de données démographiques, y compris des facteurs tels l’ethnicité, le sexe, l’âge, le statut socio-économique,…
Cette diversité et équité dans l’inclusion dans les essais cliniques représente une opportunité pour la recherche mais soulève également des défis.
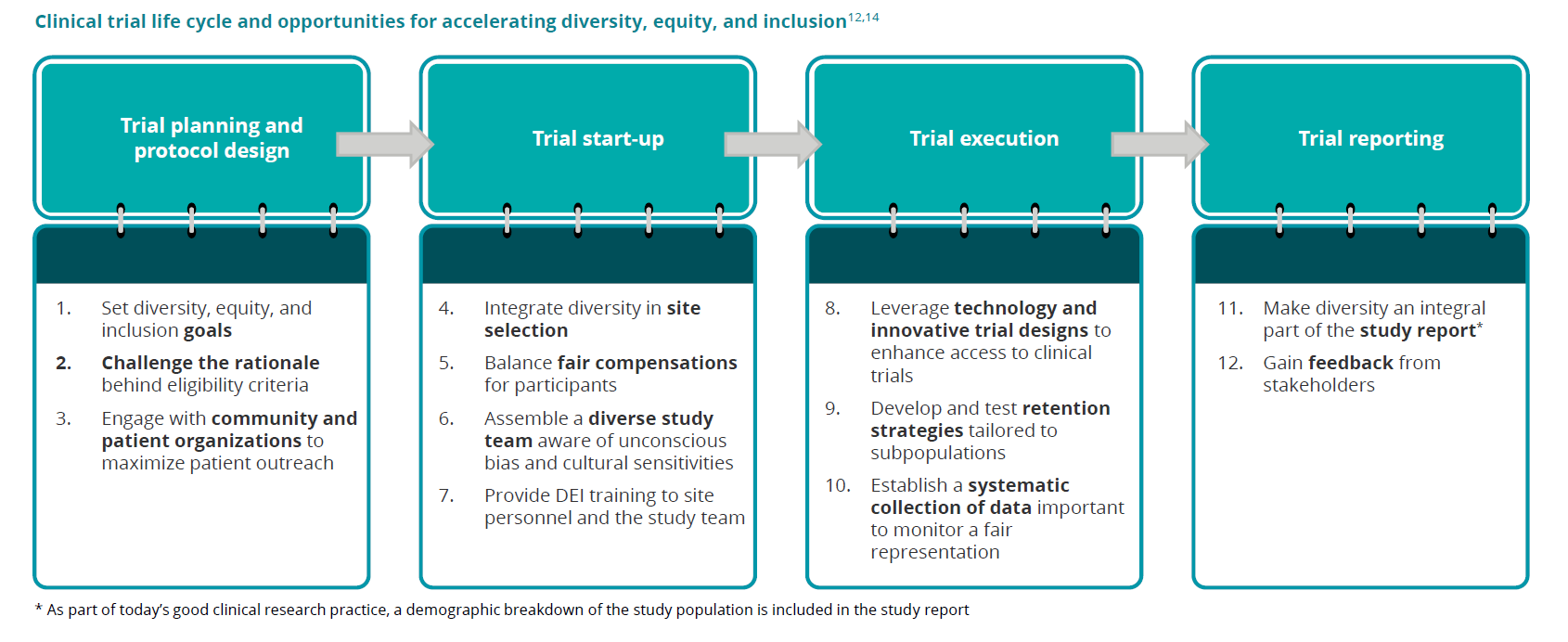
Douze recommandations ont ainsi été formulées (p.23-34) afin de garantir une approche multifactorielle tout au long du cycle de l'essai clinique.
La diversité était au cœur de notre Forum Clinical Trials annuel qui s’est tenu le 30 janvier 2024.


Intéressé(e) à recevoir les nouvelles de pharma.be
Etre au courant de ce qui vit au sein de l'industrie pharmaceutique ? Inscrivez-vous à notre lettre d'information.


