Le remboursement des médicaments innovants pourrait être amélioré en Belgique
Le rôle de pionnier de notre pays dans le développement et la production de médicaments innovants ne se traduit malheureusement pas par une mise à disposition rapide de ces innovations pour les patients.
La Belgique est à la traîne en matière de remboursement comparée à d’autres pays européens
Afin de positionner la Belgique au sein de l'Europe, nous utilisons des données sur le remboursement dans 34 pays européens, collectées par la Fédération européenne des associations et industries pharmaceutiques EFPIA. L'indicateur européen W.A.I.T. 2020 analyse le remboursement de tous les médicaments qui ont été approuvés par l'Agence européenne des médicaments (EMA) entre 2016 et 2019 et qui sont donc éligibles au remboursement dans les différents états membres européens.
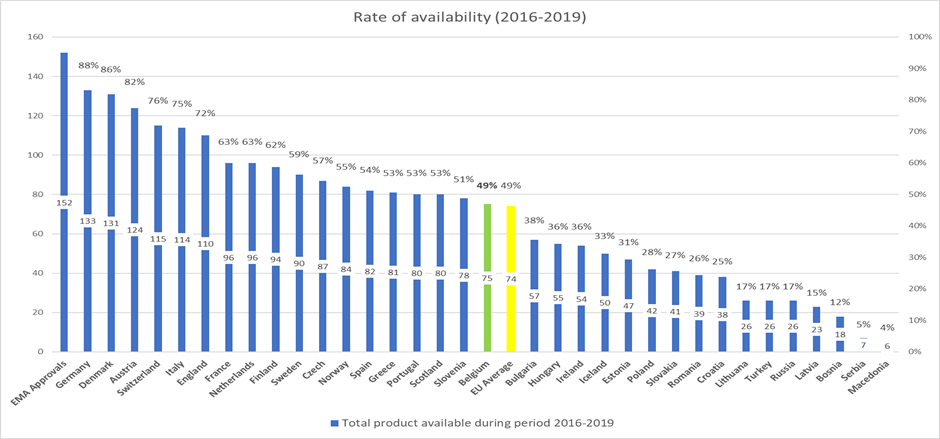
Sur les 152 médicaments étudiés, seuls 75 étaient remboursés en Belgique à la fin de 2020. Cela signifie que moins de la moitié (49%) des médicaments ayant reçu une autorisation de mise sur le marché étaient disponibles pour les patients belges. Cela nous place à la dix-huitième place. Les différences deviennent encore plus évidentes si l'on compare avec les grands pays voisins comme l'Allemagne et la France, où respectivement 88% et 64% des médicaments ont été remboursés.
Malheureusement, nous devons en conclure que les patients belges ont nettement moins accès aux médicaments innovants que les patients des pays européens comparables.
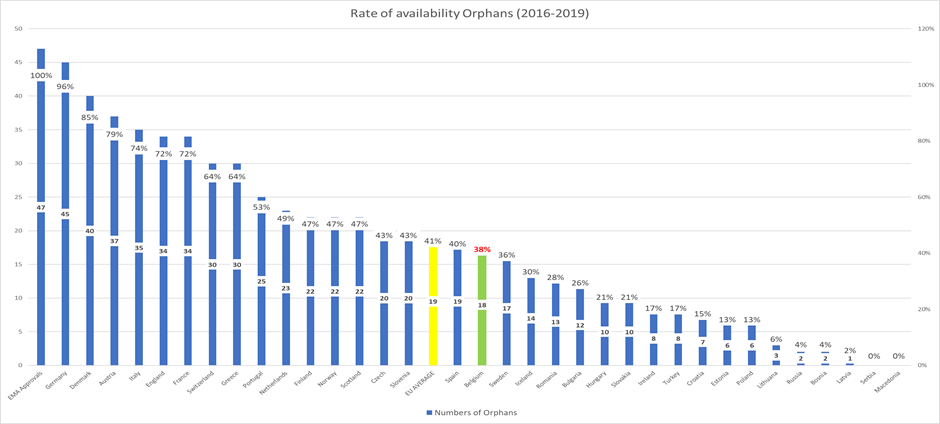
La même analyse pour les médicaments orphelins utilisés pour le traitement des maladies rares montre que la Belgique est en bas du classement avec seulement 38% des médicaments orphelins approuvés remboursés en Belgique.
Environ trois procédures de remboursement sur quatre en Belgique aboutissent à un remboursement effectif
pharma.be a analysé les procédures de remboursement abouties à la Commission de remboursement des médicaments (CRM) pour la période 2018 à 2020. L’analyse porte sur les procédures de remboursement terminées avec deux résultats possibles : soit le médicament est remboursé et dès lors disponible pour le patient, soit le remboursement a été refusé. Nous distinguons trois types de médicaments : les médicaments ayant une plus-value thérapeutique, les médicaments orphelins et les nouvelles indications.*
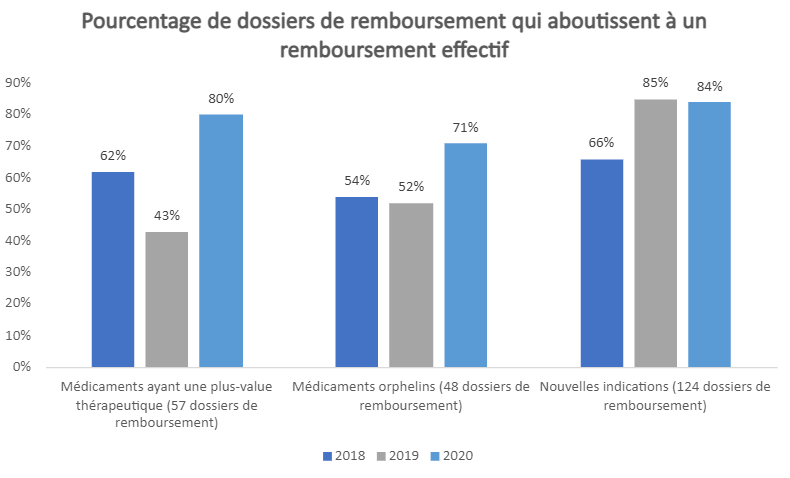
En général, environ trois quarts des demandes de remboursement d'un médicament innovant en Belgique aboutissent à un remboursement effectif.
Les chiffres pour l'année 2020 sont plus favorables mais sont moins représentatifs, car il y a eu un quart de procédures en moins en 2020 par rapport aux deux années précédentes. Cette diminution est liée à la crise du COVID-19. Pour cette raison, nous concentrons notre attention sur les résultats de 2018 et 2019.
Les médicaments ayant une plus-value thérapeutique et les médicaments orphelins ont clairement plus de difficulté à être remboursés en Belgique. Dans l'ensemble, un peu plus de la moitié des demandes de remboursement ont été approuvées en 2018 et 2019. Pour l'autre moitié des demandes, aucune décision positive n'a été prise et ces médicaments sont donc restés indisponibles pour les patients.
Les procédures de remboursement des médicaments pour de nouvelles indications ont connu une évolution positive. C'est le résultat d'une nouvelle méthode utilisée par la CRM depuis juillet 2018 pour évaluer les nouvelles indications de ces médicaments, qui porte clairement ses fruits. En 2019, 85% des demandes ont donné lieu à un remboursement.
Le remboursement prend trop de temps
Le parcours des nouveaux médicaments, du laboratoire au patient, est très long. Après des années de recherche clinique et de développement, il faut passer par une longue procédure administrative.
Avant que les patients belges puissent avoir accès à un nouveau médicament, une autorisation de mise sur le marché de l'Agence européenne des médicaments (EMA) et une décision de remboursement du Ministre belge des Affaires Sociales sont nécessaires. L'EMA a besoin d'un maximum de 210 jours pour décider de l'autorisation de mise sur le marché européen. La procédure nationale de remboursement qui s'ensuit prend également plusieurs mois, comme le montrent les chiffres ci-dessous.
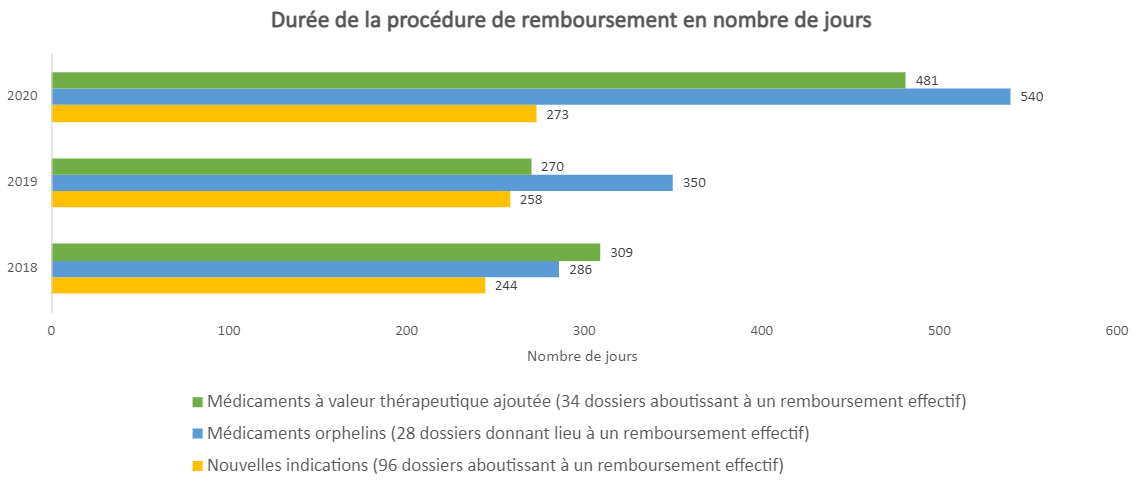
Lorsque l'on analyse le délai entre la soumission du dossier de remboursement à la Commission de remboursement des médicaments et la date à laquelle le médicament est effectivement remboursé et peut être prescrit, il apparaît que la procédure de remboursement en 2018 et 2019 prend rapidement 8 à 12 mois. Les pics en 2020 peuvent également s'expliquer ici par l'impact de la crise du COVID-19. Les patients doivent donc être très patients pour être traités avec des médicaments innovants en Belgique.
* Indications
- Selon l’entreprise pharmaceutique concernée, un médicament ayant une plus-value thérapeutique donne lieu à une valeur thérapeutique supérieure à celle d’un traitement standard reconnu. Cela signifie que la maladie est mieux traitée avec ce médicament.
- Un médicament orphelin est un médicament destiné au traitement d’une maladie rare et offre donc souvent une solution à un besoin médical non satisfait.
- Une nouvelle indication fait référence à un médicament qui est déjà remboursé pour une certaine indication/affection et pour lequel la société demande un remboursement supplémentaire pour une autre indication/affection. Il pourrait s’agir, par exemple, d’un médicament déjà remboursé pour le traitement du cancer du poumon, mais qui est désormais également remboursé pour le traitement du cancer colorectal.



Intéressé(e) à recevoir les nouvelles de pharma.be
Etre au courant de ce qui vit au sein de l'industrie pharmaceutique ? Inscrivez-vous à notre lettre d'information.


